CONCEPTOS BÁSICOS
Energía: es la capacidad para realizar o para transferir calor. Su unidad en el Sistema Internacional es el joule (J)
Trabajo (W): es la energía utilizada para mover un objeto contra una fuerza. Depende de la fuerza aplicada y la distancia recorrida. Su fórmula es
W = Fuerza x distancia.
Calor (q): es la energía empleada para incrementar una temperatura de un objeto. Se transfiere de un objeto más caliente hacia uno más frío.
Energía Interna (E): suma de todas las energías (cinéticas y potenciales) de las partículas que forman un sistema.
Energía cinética (Ek): es la energía asociada al movimiento. Depende de su masa (m) y velocidad (v). Su formula es
Ek = ½ · m · v2
Energía potencial (Ep): energía en virtud de la posición de un objeto con respecto a otros objetos, Depende de su masa (m), la altura (h) relativa respecto al suelo y a la gravedad (g=9,8 m/s2).
Ep = g · m · h
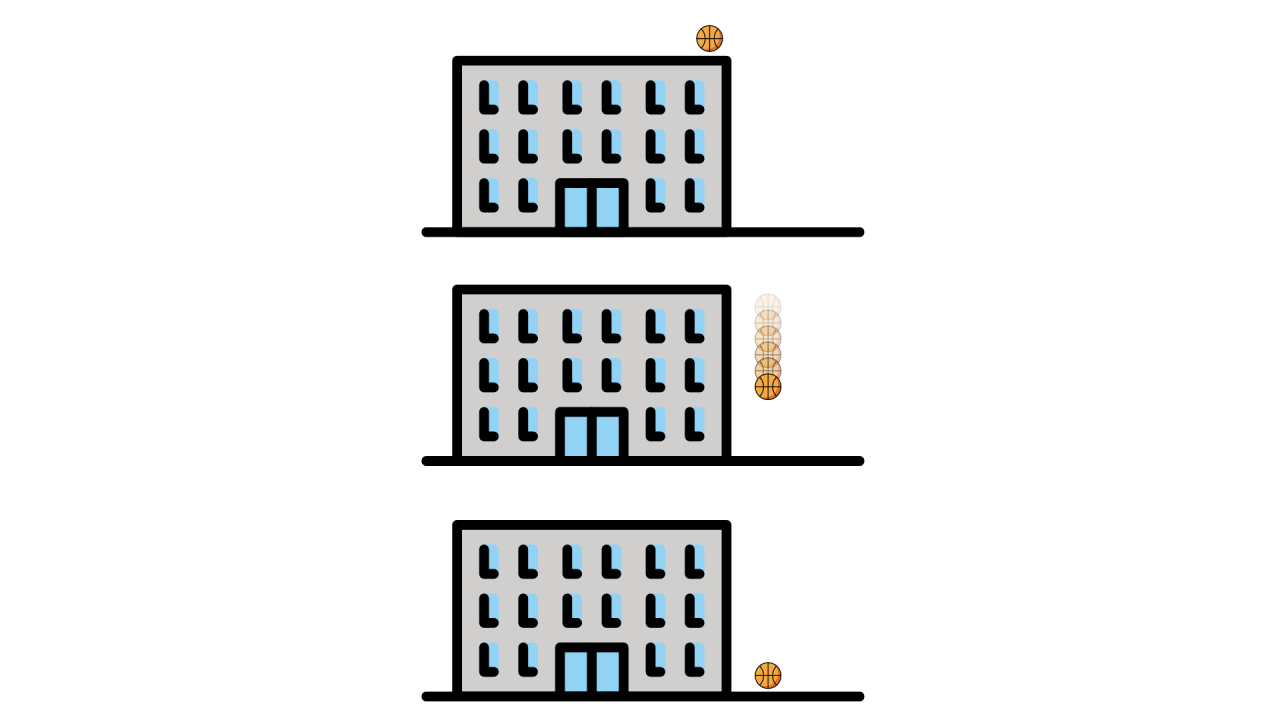
Relación general de la energía
El cambio en la energía de un sistema se expresa como:
ΔE = W + q
SISTEMA Y SU ENTORNO
Sistema: parte limitada y bien definida del universo escogida para su estudio.
Entorno: resto del universo.
En una reacción química los reactivos y los productos constituyen el sistema, el recipiente y todo lo demás se considera su entorno.
TIPOS DE SISTEMAS
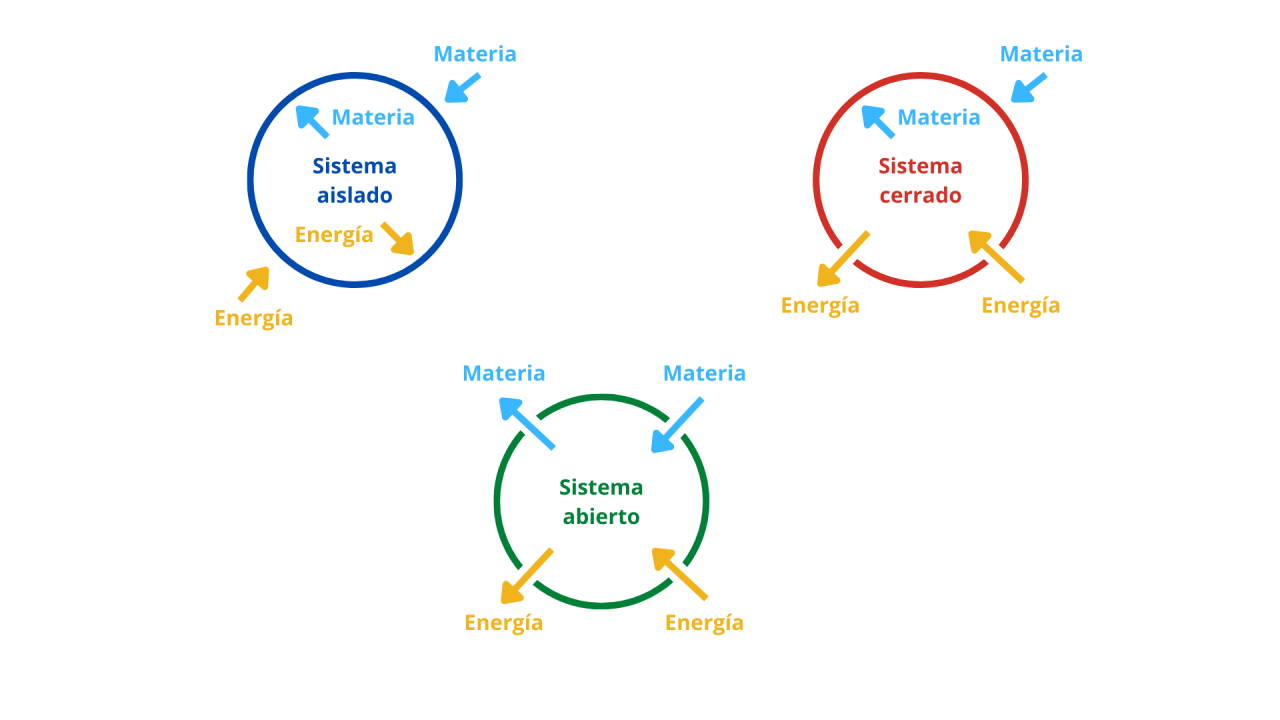
Sistema abierto: sistema donde la materia y la energía se pueden intercambiar con el entorno.
Sistema cerrado: sistema en el que hay intercambio de energía, pero no de materia.
Sistema aislado: no hay intercambio de energía ni de materia con el entorno.
Sistema Adiabático: sistemas que conservan la temperatura en periodo de tiempo corto, pueden intercambiar materia.
TRANSFERENCIA DE ENERGÍA (TRABAJO Y CALOR)
Primera Ley de la Termodinámica: “Cualquier energía perdida por un sistema debe ganarla su entorno y viceversa”.
Cambio en la energía interna: ΔE = Efinal - Einicial
ΔE = q + W
ΔE > 0 cuando Efinal > Einicial significa que el sistema ganó energía de su entorno.
ΔE < 0 cuando Efinal < Einicial significa que el sistema perdió energía de su entorno.
CONVENCIÓN DE SIGNOS
| Calor (q) | (+) sistema gana calor | (-) sistema pierde calor |
| Trabajo (W) | (+) trabajo realizado sobre el sistema | (-) trabajo realizado por el sistema |
| Cambio de energía interna (ΔE) | (+) ganancia neta por el sistema | (-) pérdida neta por el sistema |
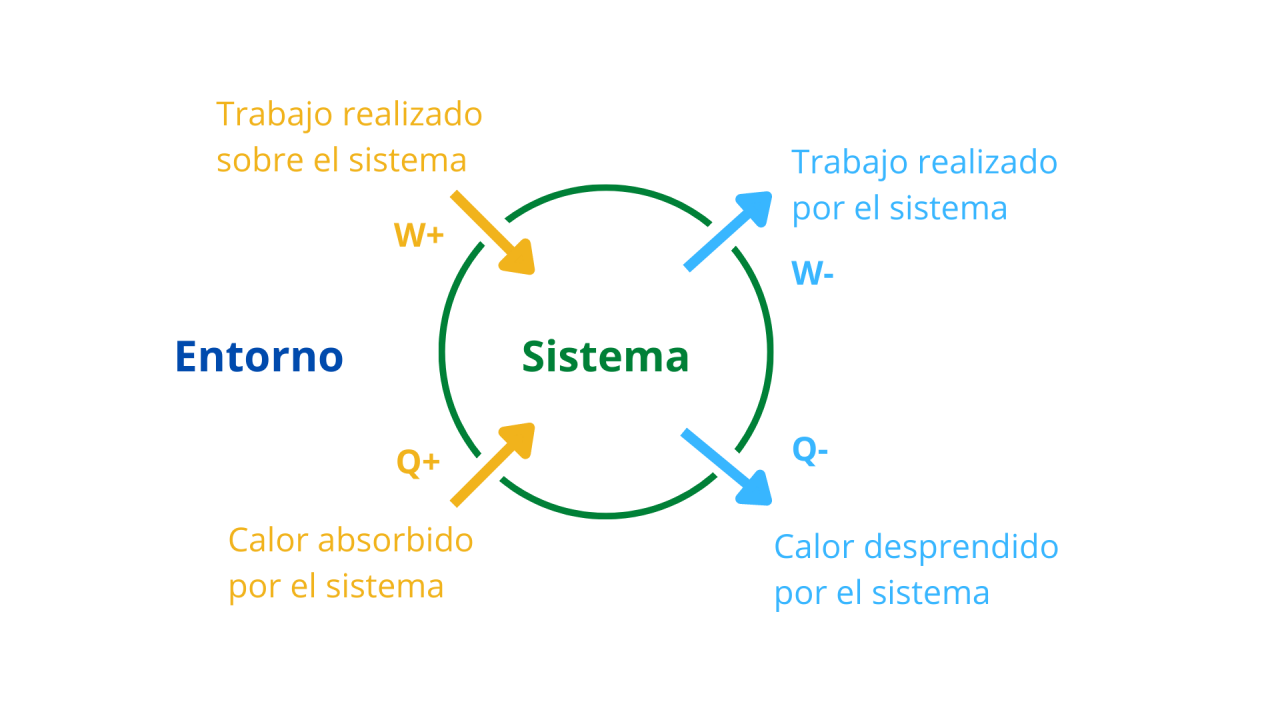
Proceso endotérmico: El sistema absorbe calor de su entorno.
Proceso exotérmico: El sisitema pierde calor y lo libera a su entorno.
FUNCIÓN DE ESTADO
El valor de una función de estado solo depende del estado actual de un sistema, no de la trayectoria que el sistema siguió para llegar a dicho estado. Solo depende de los estados inicial y final. La energía es función de estado, el calor y el trabajo NO son funciones de estado.
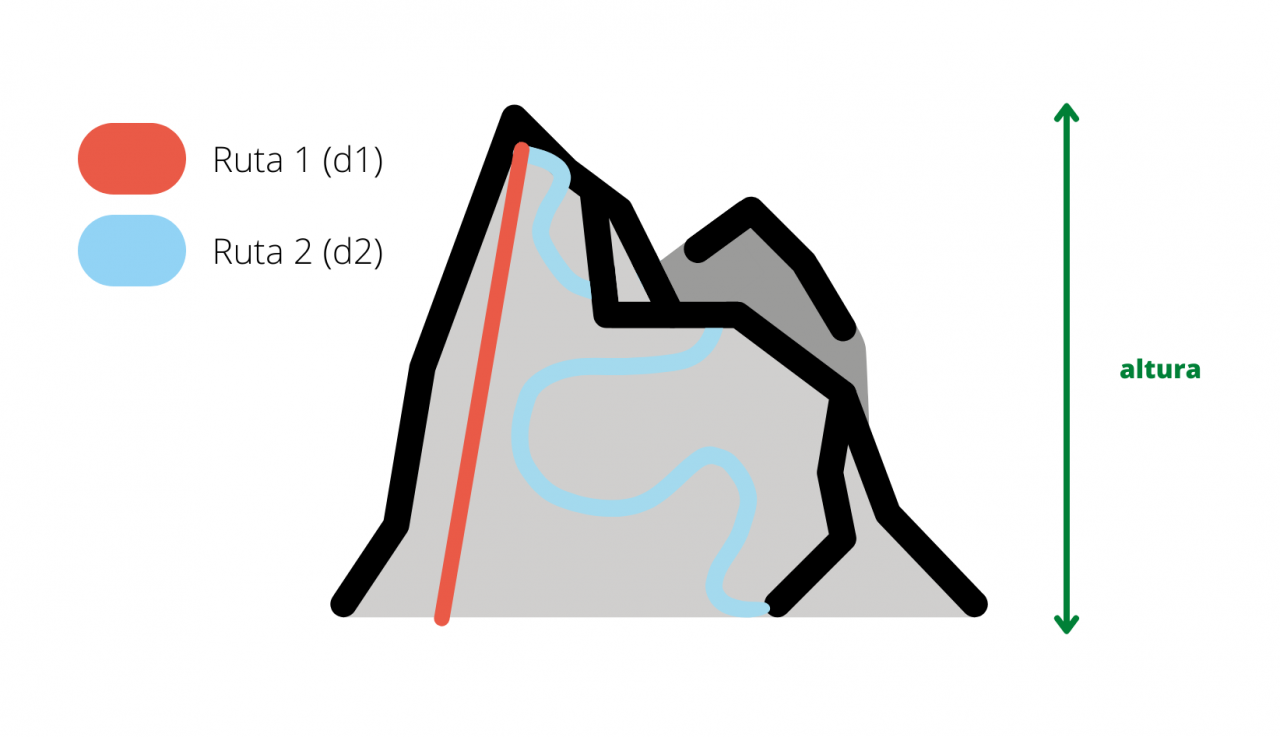
Ejemplo para explicar función de estado: dos caminantes suben a la misma altura de la montaña (h) partiendo de un mismo punto. Al llegar a la cima, la altura (h) sería la misma para ambos caminantes independientemente del camino seguido por cada uno, por lo tanto, h es función de estado en este ejemplo. Por otro lado, las distancias d1 y d2 sí dependen de la trayectoria seguidas, pues d1 ≠ d2, por lo que no serían funciones de estado.
PRÁCTICA
Ambos negativos (-)
ΔE = +220 J
Negativo. ΔE = -400 J
Debe abosrber calor (q positivo)
Se realizó trabajo sobre el sistema (W positivo)
Positivo. El sistema gana energía
AUTORES
Fabio Araya-Carvajal, Esteban Arce-Campos y Cristian Nájera-Obando