ENLACE IÓNICO
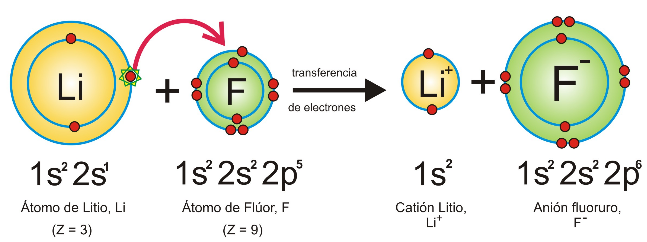
El término enlace iónico se refiere a las fuerzas electrostáticas que existen entre iones con carga opuesta. Es la unión entre elementos cargados eléctricamente con cargas opuestas. Este tipo de enlace ocurre generalmente entre metales y no metales (cuya diferencia de electronegatividad sea mayor a 1,62). Los átomos transfieren electrones completamente, pudiendo ser uno o más electrones los que se transfieren. Hay transferencia de electrones de un átomo a otro. Se originan iones positivos y negativos. En la figura se muestra una representación del enlace en el LiF. Ambos iones adquieren la configuración de un gas noble.
Naturaleza del enlace: Atracción electrostática entre iones de carga opuesta. El enlace no es dirigido; cada ion es atraído por varios iones de carga opuesta. Forma agregados de iones
PROPIEDADES DE LOS COMPUESTOS IÓNICOS
- Puntos de fusión y ebullición elevados (es necesario romper la red cristalina tan estable por la cantidad de atracciones electrostáticas entre iones de distinto signo).
- Son sólidos a temperatura ambiente.
- Gran dureza.
- Solubilidad en disolventes polares e insolubilidad en disolventes apolares.
- Conductividad en estado disuelto o fundido. Sin embargo, en estado sólido no conducen la electricidad.
- Son frágiles.