"Toda medición es una comparación de algún objeto o fenómeno, con otro aceptado como patrón"
CONCEPTOS BÁSICOS
Toda medida consta de:
Magnitud: Número que indica cuántas veces o partes del patrón, tiene lo medido.
Dimensión: Letras que especifican cuál(es) patrón(es) se ha(n) escogido para la medida.
En el Sistema Internacional, las unidades están clasificadas de acuerdo con su: complejidad, origen o uso. Las unidades son: básicas, suplementarias, derivadas, toleradas, entre otras.
Unidades básicas:
En el siguiente cuadro se denotan:
| Nombre | Símbolo | Dimensión |
| Ampere | A | Intensidad de corriente eléctrica |
| Candela | cd | Intensidad luminosa |
| Kelvin | K | Temperatura |
| Kilogramo | kg | Masa |
| Metro | m | Longitud |
| Mole | mol | Cantidad de sustancia |
| Segundo | s | Tiempo |
Múltiplos y submúltiplos de las Unidades del SI
Dentro del Sistema Internacional sólo se permiten múltiplos y submúltiplos que varíen en potencias de 10-3 o 103. A continuación se denota de forma tabular los diferentes múltiplos y submúltiplos del SI:
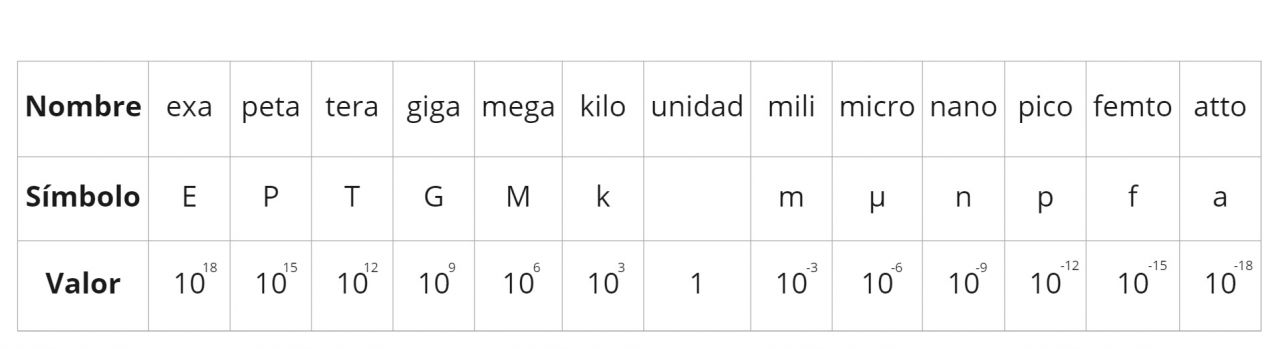
Unidades Derivadas: Hay ocho categorías o clases, algunos ejemplos se indican en el siguiente cuadro:
| Nombre | Coulomb | Grado Celsius | Joule | Newton | Pascal |
| Símbolo | C | ºC | J | N | Pa |
| Equivalente | A×s | K-273.15 | m2×kg/s2 | kg×m/s2 | kg/(m×s2) |
| Dimensión | Cantidad de electricidad | Temperatura | Energía | Fuerza, peso | Presión |
Unidades Toleradas: Son algunas unidades de uso común y sólo se pueden combinar con unidades básicas. Ejemplo: día, hora (h), minuto (min) y litro (L).
Unidades Admitidas Temporalmente: Comprende algunas unidades muy usadas en algunas disciplinas. Algunas son: ångström (Å), bar (bar) y hectárea (ha).
Unidades Especiales: Son el electronvolt (eV) y la unidad de masa atómica unificada (u), que dependen de algún valor experimental, susceptible de ser determinado cada vez más exactamente.
Unidades Prohibidas: Son unidades que pertenecen a otros sistemas diferentes del S.I. Algunos ejemplos: ergio y caloría (para energía), dina (para fuerza), libra-fuerza por pulgada cuadrada y atmósferas (para presión), libra y onza (para masa), milla, pie y pulgada (para longitud), galón y onza fluida (para volumen), etc.
FACTORES DE CONVERSIÓN
Un factor es "cada una de las cantidades o expresiones algebraicas que se multiplican una por otra para obtener un producto". Los factores de conversión unitarios corresponden a multiplicandos (factores) iguales a la unidad. Siempre se obtienen de una igualdad o equivalencia.
Hay factores adimensionales (sin unidades) que corresponden a proporciones, como cuando se afirma que es la mitad o el triple de algo.
Casi la totalidad de los factores de conversión que empleamos tienen dimensión (con unidades); estas siempre se escriben de acuerdo con las reglas del S.I. Si las unidades empleadas no son del S.I., se usa el nombre de la unidad o el símbolo aceptado comúnmente en español. Por ejemplo, libra (lb), tonelada (ton), pulgada (pulg), pie, milla y onza.
Según el S.I. no hay que mezclar nombre y símbolos. Por razones de espacio, en los cálculos se usan los símbolos de las unidades.
Cuando se trabaja con cantidades, volúmenes o masas de sustancias químicas, además de especificar la unidad, hay que escribir como subíndice el símbolo o fórmula química. Si esta sustancia tiene alguna característica adicional, por ejemplo: pura, teórica, concentrada, impura, etc., también se indica.
Ejemplos: 8x1028 átomo Au, 21 m3 NaBr, 5 kg HClconc., 740 lb CaOimpuro.
Algunas equivalencias entre unidades: En el siguiente cuadro se indican algunas equivalencias entre unidades:
Dimensión | Unidad SI | Equivalencia en otras unidades |
| Energía | Joule (J) | 1 J = 0,24 caloría = 107 ergios = 9.9×10-3 litro-atmósfera = 2,8×10-7 kilowatt-hora |
| Longitud | Metro (m) | 1 m = 1010 ángstroms = 6.2×10-4 milla = 3.28 pies = 1.09 yardas = 39,37 pulgadas |
| Masa | Kilogramo (kg) | 1 kg = 2.2 libras = 35.27 onzas = 10-3 tonelada métrica = 6.02×1026 unidades de masa atómica |
| Presión | Pascal (Pa) | 1 Pa = 0.87×10-6 atmósfera = 1.45×10-4 libra-fuerza por pulgada cuadrada |
| Temperatura | Kelvin (K) | 1 K = 273,15 + grado Celsius = 0.56 × (Farenheit - 32)+ 273,15 |
| Tiempo | Segundo (s) | 1 s = 3.17×10-8 año = 1.16×10-5 día = 2.8×10-4 hora = 1.7×10-2 minuto |
| Volumen | Metro cúbico (m3) | 1 m3 = 103 litros = 35.31 pies cúbicos = 6.1×104 pulgadas cúbicas |
TRABAJANDO CON FACTORES DE CONVERSIÓN
En el análisis dimensional, se utilizan unidades en todos los cálculos. Las unidades se multiplican unas por otras, se dividen unas entre otras o se “cancelan”. El análisis dimensional ayuda a asegurar que las soluciones a los problemas tengan las unidades correctas. Además, el análisis dimensional ofrece una forma sistemática de resolver muchos problemas numéricos y de revisar las soluciones para detectar posibles errores.
La clave para usar el análisis dimensional es el empleo correcto de factores de conversión para transformar una unidad en otra. Un factor de conversión es una fracción cuyo numerador y denominador son la misma cantidad expresada en diferentes unidades. Por ejemplo, 2.54 cm y 1 pulg son la misma longitud, 2.54 cm = 1 pulg. Esta relación nos permite escribir dos factores de conversión:
![]()
Usamos el primero de estos factores cuando queremos convertir pulgadas en centímetros. Por ejemplo, la longitud en centímetros de un objeto que tiene 8,50 pulg de largo está dada por:
![]()
Las unidades de pulgadas en el denominador del factor de conversión se cancelan con las unidades de pulgadas en el dato que se nos da (8,50 pulgadas). Los centímetros en el numerador del factor de conversión se convierten en las unidades de la respuesta final. Dado que el numerador y el denominador de un factor de conversión son iguales, multiplicar cualquier cantidad por un factor de conversión equivale a multiplicar por 1, lo cual no altera el valor intrínseco de la cantidad. La longitud 8,50 pulg es la misma que 21,6 cm.
En general, iniciamos cualquier conversión examinando las unidades del dato dado y las unidades que queremos. Luego nos preguntamos con qué factores de conversión contamos para ir de las unidades de la cantidad dada a las de la cantidad deseada. Cuando multiplicamos una cantidad por un factor de conversión, las unidades se multiplican y dividen como sigue:
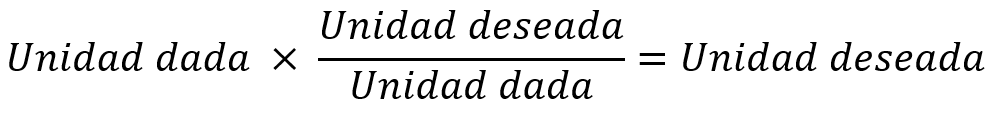
Si no se obtienen las unidades deseadas en un cálculo, forzosamente se cometió un error en algún punto. La inspección cuidadosa de las unidades a menudo revela la fuente del error.
Ejercicio: Si una mujer tiene una masa de 115 lb, ¿Qué masa tiene en gramos?
Solución Dado que queremos pasar de lb a g, buscamos una relación entre estas unidades de masa. Así 1 lb = 453,6 g. Para cancelar las libras y dejar gramos, usamos el factor de conversión que tiene gramos en el numerador y libras en el denominador:
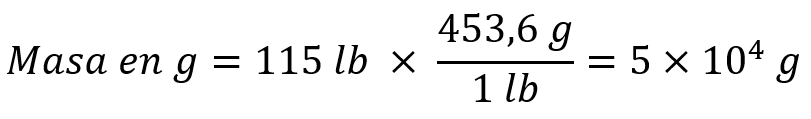
USO DE DOS O MÁS FACTORES DE CONVERSIÓN
Con frecuencia es necesario usar más de un factor de conversión en la resolución de un problema. Por ejemplo, supongamos que nos interesa conocer la longitud en pulgadas de una varilla de 8.00 m. La relación entre centímetros y pulgadas (1 pulg = 2.54 cm) y, por lo que hemos aprendido de los prefijos métricos, sabemos que 1 cm = 10-2 m. Por tanto, podemos efectuar la conversión paso por paso, primero de metros a centímetros y luego de centímetros a pulgadas. Al combinar la cantidad dada (8.00 m) con los dos factores de conversión, tenemos:
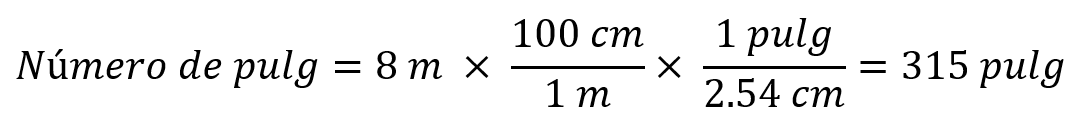
Al aplicar el primer factor de conversión para cancelar metros y convertir la longitud en centímetros. Por ello, se escribe metros en el denominador y centímetros en el numerador. El segundo factor de conversión debe cancelar centímetros, así que tiene centímetros en el denominador y pulgadas, la unidad deseada, en el numerador.
También se tienen factores de conversión que convierten de una medida a otra. Supongamos que nos interesa conocer la masa en gramos de dos pulgadas cúbicas (2,00 pulg3) de oro, que tiene una densidad de 19,3 g/cm3. Dado que la respuesta deseada es una masa en gramos, es evidente que necesitaremos el primero de estos factores, que tiene masa en gramos en el numerador. Sin embargo, para poder usar este factor necesitaremos convertir primero pulgadas cúbicas en centímetros cúbicos. La relación entre pulg3 y cm3 no está dada en tablas, pero sí la relación entre pulgadas y centímetros: 1 pulg = 2,54 cm (exactamente). Si elevamos al cubo ambos miembros de esta ecuación, tendremos (1 pulg)3 = (2.54 cm)3, de donde podemos obtener el factor de conversión deseado para resolver el problema.
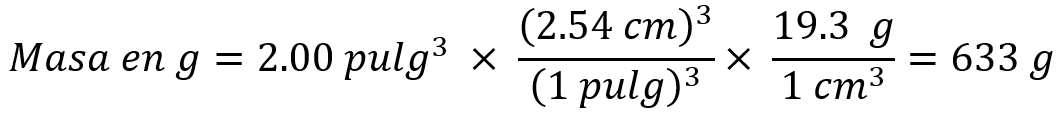
No haga cálculos intermedios. Esto es: multiplicar dos factores, escribir resultado, éste multiplicarlo por otro factor, y así sucesivamente. Este procedimiento incorrecto; genera valores diferentes del real pues cada resultado intermedio se redondea. En todo caso, se considera como una serie de reglas de tres disfrazadas.
LAS RELACIONES PARA CAMBIOS EN TEMPERATURA (ΔT):
Aunque sí aparecen las conversiones entre dos escalas de temperatura, estas siempre involucran sumas y restas, por lo que no es posible emplearlas en un factor de conversión. Según se ve en la figura 1.8, al comparar termómetros con diferentes escalas, K, °C y °F, una temperatura absoluta cambia su valor, además de que la relación en las diferencias de temperatura no son las mismas en las diferentes escalas, solamente es factible usar como un factor los cambios en temperatura (ΔT), cuando así se especifica; si no, se deja sin convertir la unidad de temperatura.
ΔT = 1 K = °C = 1,8 °F
Cuando se quiere interconvertir una temperatura absoluta de una escala a otra se usan las siguientes fórmulas:
De Kelvin a Celsius C = K - 273.15 | De Celsius a Kelvin K = C + 273.15 |
De Fahrenheit a Celsius C = 5 × (F - 32)/9 | De Celsius a Fahrenheit F = 9C/5 + 32 |
De Kelvin a Fahrenheit F = 9 (K -273.15)/5 + 32 | De Fahrenheit a Kelvin K = 5 × (F -32)/9 + 273.15 |
Si por otra parte se trabaja con cambios en la temperatura y se quiere interconvertir entre dos escalas se debe usar la siguiente relación:
1 K = 1 °C = 1,8 °F
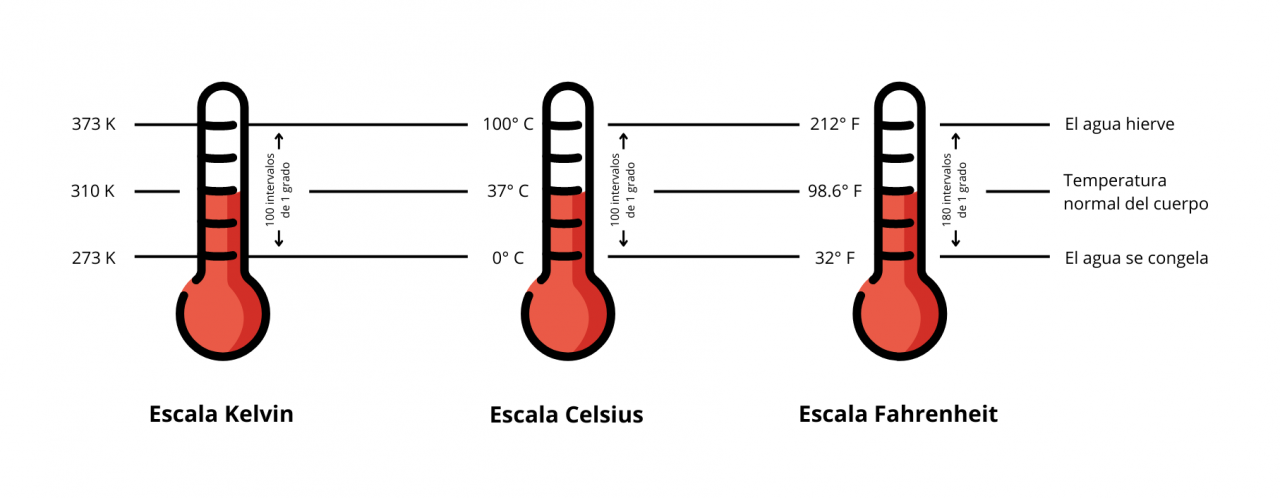
Diferentes escalas de temperatura
EJEMPLO
Ejemplo: si se coloca una muestra de acetona a 90°F en un vidrio de reloj y después de que se evapora la temperatura del vidrio se reduce 7°C ¿cuál será la temperatura final de vidrio en K?
Datos del problema
Temperatura inicial (Ti) = 90 °F
Cambio de temperatura (ΔT) = -7 °C
| Método de resolución A | Método de resolución B |
Convertir la temperatura absoluta a otra escala Ti = 90 °F Ti = 5/9 (90 - 32) = 32,22 °C ΔT = Tf - Ti Tf = ΔT + Ti = -7 °C + 32,22 °C = 25,22 °C Tf = 25,22 + 273 = 298,22 K | Convertir el cambio de temperatura a otra escala ΔT = - 7° C x 1,8 °F / °C = -12,6 °F ΔT = Tf - Ti Tf = ΔT + Ti = -12,6 °F + 90 °F = 77,4 °F Tf= 5/9 (77,4 – 32) = 25,22 °C Tf = 25,22 + 273 = 298,22 K |
Aunque se usan diferentes métodos se llega al mismo resultado: 298,22 K. Lo importante es encontrar cuándo se habla de una temperatura absoluta y cuándo un cambio en la temperatura para usar las fórmulas de conversión correctas en cada caso.
EXACTITUD Y PRECISIÓN EN LAS MEDICIONES
Exactitud: cuán cercana está una medición del valor real de la cantidad medida.
Precisión: cuánto concuerdan dos o más mediciones de una misma cantidad.
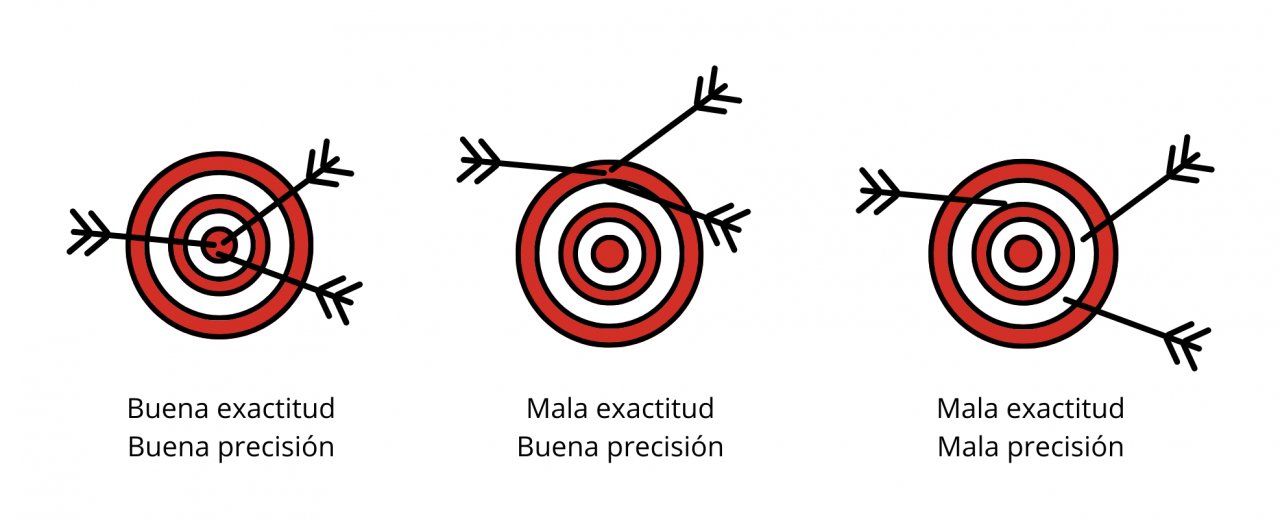
Esquema explicativo de exactitud y precisión.
CIFRAS SIGNIFICATIVAS
Son todos los dígitos ciertos más el primer dígito incierto de un dato o un resultado numérico, o dicho de otra forma son todas aquellas cifras que se conocen con certeza más la primera cifra incierta. Por ejemplo, si la medición de una masa dio 15,38 g, éste dato tiene 4 cifras significativas, tres que se conocen con certeza y la incierta que es el 8.
Los datos y resultados experimentales para reportarlos se deben expresar con el número de cifras significativas correctas. Este número de cifras significativas es dado por la incertidumbre absoluta del dato o el resultado numérico de la operación matemática, que más adelante se explica.
Sin embargo, no es lo mismo anotar la masa de un objeto como 1,00 g que como 1,0000 g. En el primer caso el dato tiene tres cifras significativas y en el segundo cinco, lo cual significa que conocemos con mayor certeza la segunda masa. El número de cifras significativas está determinado en este caso por el tipo de balanza utilizada. Tampoco puede decirse que la masa del objeto es "exactamente" 1 g o exactamente 1,00 g o 1,0000 g, porque toda medición difiere en mayor o menor grado del valor real.
El cero en un dato o resultado numérico puede o no ser una cifra significativa, dependiendo de su localización en el número:
- El cero que está rodeado por otros dígitos siempre es significativo. Ejemplo, en 32,05 g hay 4 cifras significativas.
- Los ceros que sólo sitúan la como decimal no son significativos, o sea aquellos ceros después de la coma, por ejemplo, en 30,24 mL hay 4 cifras significativas y si la escribimos en litros como 0,03024 L, el número de cifras significativas no varía, siguen siendo 4.
- Los ceros al final pueden ser o no ser significativos. Por ejemplo, si el volumen de un vaso se expresa como 2,0 L el cero nos indica que el volumen se conoce hasta décimas de litro; así, tanto el 2 como el 0 son cifras significativas. En el caso de querer expresar este mismo volumen en mililitros, se debe utilizar la notación científica para mantener en dos cifras significativas el volumen, se expresaría entonces como 2,0 x 103 mL. Si se escribiera este volumen como 2000 mL tendría cuatro cifras significativas en lugar de dos.
- El cero es cifra significativa en números exactos, como en el caso de datos que se obtienen por conteo. Por ejemplo, la palabra “disolución” tiene 10 letras exactas.
REDONDEO
En muchos casos es necesario redondear el resultado, para obtener la cantidad de cifras significativas correctas y se deben eliminar los últimos dígitos. Para ello, se deben utilizar los siguientes criterios de redondeo:
- Si el primer dígito que debe suprimirse es menor que 5, el último dígito que se conserva permanece sin cambiar. Por ejemplo, la cantidad 1,223 se expresa con tres cifras significativas como 1,22.
- Si el primer dígito a eliminarse es mayor que 5, el último dígito que se conserva se incrementa en una unidad. Por ejemplo, la cantidad 1,228 se expresa con tres cifras significativas como 1,23.
- Si el dígito a eliminarse es 5 y los siguientes son diferentes de cero, el último dígito que se conserva se aumenta en una unidad. Por ejemplo, la cantidad 21,8653 expresada con cuatro cifras es 21,87.
- Si el dígito a eliminarse es 5 y los siguientes son ceros, el último dígito que se conserva no cambia si es par y aumenta en una unidad si es impar. Por ejemplo, la cantidad 0,68500 expresada con dos cifras significativas es 0,68 debido a que el 8 es par y en la cantidad 0,63500 expresada con dos cifras significativas es 0,64 debido a que el 3 es impar y se debe aumentar en una unidad.
VIDEOS
Química General : Factores de Conversión
Química Básica 1 : Ejercicio para pasar de unidades derivadas a unidades básicas
Química : Ejercicios de conversión de unidades
Química General : Conversión de Temperaturas
Química : Ejercicios de escala de temperaturas
PRÁCTICA
AUTORES
Fabio Araya-Carvajal, Esteban Arce-Campos y Cristian Nájera-Obando